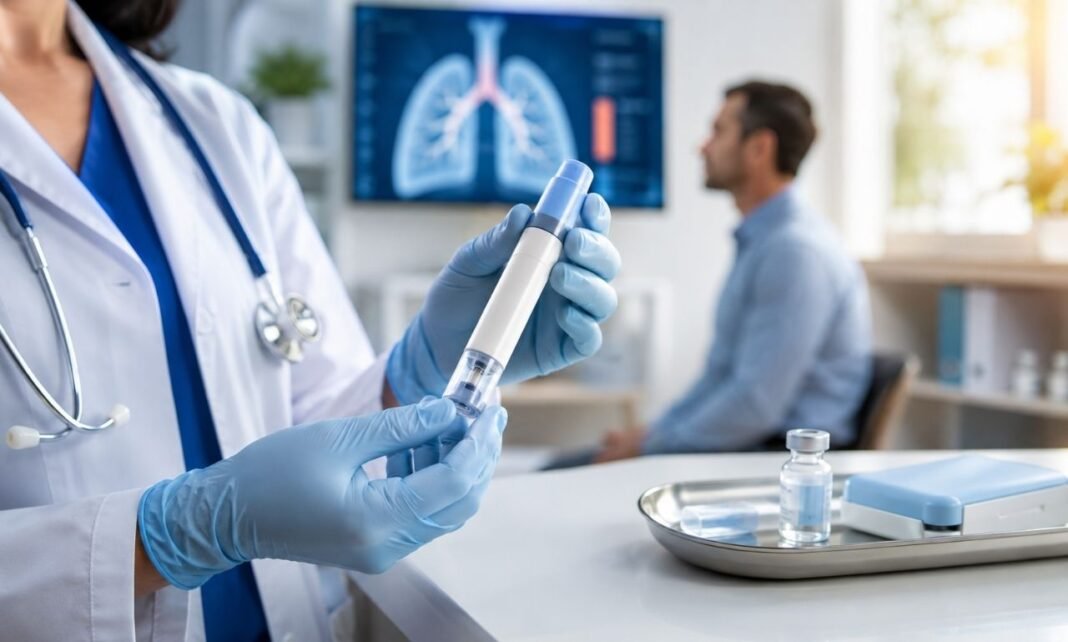
Medicamento para doenças respiratórias foi aprovado pela Agência Nacional de Vigilância Sanitária para o tratamento de quadros específicos de asma e rinossinusite crônica com pólipos nasais grave. O produto, chamado Densurko, tem como princípio ativo o depemoquimabe e será apresentado como solução injetável.
A aprovação foi publicada pela Anvisa na segunda-feira, 11 de maio de 2026. Segundo as informações divulgadas, o medicamento será usado em adultos e adolescentes acima de 12 anos e terá aplicação a cada 6 meses, sempre conforme a indicação prevista para cada condição.
Medicamento para doenças respiratórias tem uso injetável
O medicamento para doenças respiratórias aprovado pela Anvisa é apresentado como solução injetável de 100 mg/mL. De acordo com a publicação, o produto estará disponível em seringa preenchida ou caneta aplicadora, ambas prontas para uso.
A indicação envolve situações de maior gravidade, especialmente quando há relação com inflamação eosinofílica. Esse tipo de inflamação pode estar associado ao agravamento de quadros respiratórios e ao aumento do risco de crises relevantes de asma.
No caso da asma, os estudos clínicos citados pela divulgação apontaram redução estatisticamente significativa na taxa de exacerbações importantes, quando o medicamento foi comparado ao placebo. Em ambos os grupos, o uso ocorreu associado ao tratamento padrão.
Do registro ao uso previsto
A aprovação segue uma lógica regulatória: primeiro vem o registro, depois a indicação delimitada e, por fim, a forma de aplicação descrita para o tratamento.
A agência publicou o registro do Densurko em 11 de maio de 2026.
O uso envolve asma e rinossinusite crônica com pólipos nasais grave.
A dose indicada é de uma aplicação a cada 6 meses.
Rinossinusite crônica com pólipos também está na indicação
Além da asma, o medicamento para doenças respiratórias também foi aprovado para rinossinusite crônica com pólipos nasais em pacientes adultos. Nesse caso, a indicação é restrita a situações em que a terapia convencional, com corticosteroides sistêmicos, e/ou cirurgia não proporcionou controle adequado do quadro.
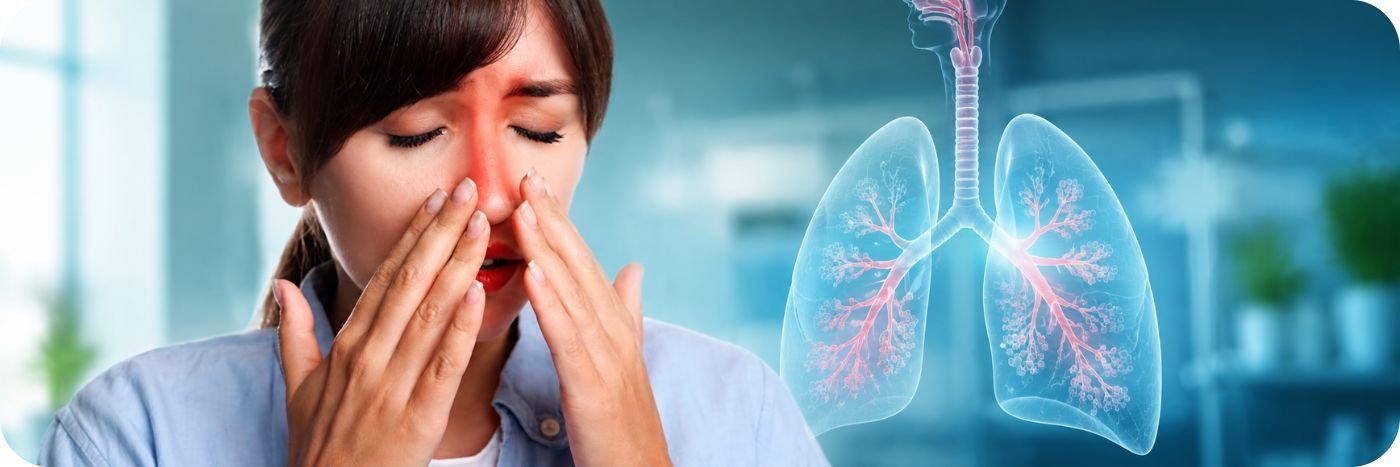
A rinossinusite crônica com pólipos nasais é descrita como uma inflamação persistente da mucosa nasal e dos seios da face. A condição tem duração superior a 12 semanas e se caracteriza pelo crescimento de pólipos benignos, que podem bloquear a respiração.
Para esse grupo, a dose indicada também segue o mesmo intervalo: uma aplicação a cada 6 meses. Assim, o ponto central da aprovação está no uso semestral em quadros graves e delimitados pelas condições previstas no registro.
O que muda com o medicamento para doenças respiratórias
O principal efeito editorial da aprovação está na ampliação do conjunto de terapias registradas para quadros respiratórios graves e específicos. O medicamento para doenças respiratórias não foi apresentado como tratamento amplo para todos os casos de asma ou rinossinusite, mas como opção ligada a perfis definidos de pacientes.
Na asma, a divulgação destaca a redução de exacerbações significativas nos estudos clínicos. Na rinossinusite crônica com pólipos nasais, a indicação se volta a adultos que não tiveram controle adequado com tratamento convencional e/ou cirurgia.
Com isso, a aprovação reforça a importância do registro sanitário para organizar a entrada de novas terapias no mercado. A informação também ajuda pacientes e familiares a compreenderem que medicamentos desse tipo seguem critérios técnicos de indicação, forma de apresentação, dose e acompanhamento.
A consequência principal da aprovação
O registro acrescenta uma opção injetável de aplicação semestral para indicações respiratórias graves e específicas.
A informação parte da publicação do registro pela Anvisa.
O tratamento aparece associado a quadros específicos e graves.
A aplicação informada é de uma dose a cada 6 meses.
Registro foi divulgado pela Anvisa
O texto original foi publicado pela Anvisa em 11 de maio de 2026 e adaptado pelo Poder360. A divulgação informa que o conteúdo é livre para republicação, desde que a fonte seja citada.
Portanto, a notícia deve ser lida como uma informação regulatória sobre aprovação de medicamento. O medicamento para doenças respiratórias recebeu registro para usos específicos, com apresentação injetável e aplicação semestral, dentro das condições descritas pela agência.